中国首款糖尿病ED干细胞新药获批,深圳再生引领细胞治疗革命
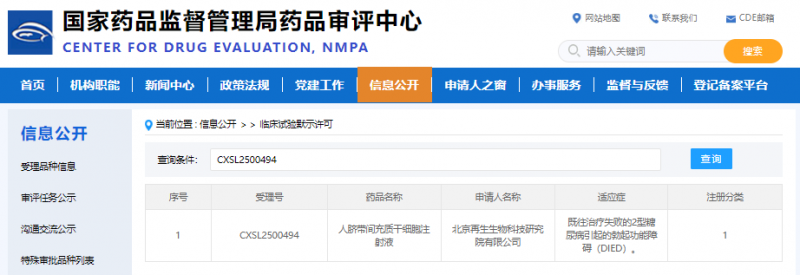
▲截图来自 CDE 官网
破局临床痛点,深圳再生抢占千亿蓝海市场
作为糖尿病最棘手的并发症之一,糖尿病ED因长期高血糖损伤阴茎海绵体神经与血管,导致传统PDE5i类药物对患者疗效不佳或无效,临床治疗长期陷入“无药可用”的困境。而北京细胞研究院研发的BJZS001,在靶向修复缓解血管神经损伤、从根源改善功能和高安全性三个方面具有核心优势,为患者带来治疗新希望。

▲北京再生细胞研究院
目前,我国糖尿病患者达2.33亿,男性患者中63.6%受ED困扰。据第三方测算显示,2028年国内糖尿病ED治疗市场规模将突破600亿元,整体市场空间可达千亿级。此次BJZS001获得临床试验默示许可,也有望打开这样一个被长期压抑的巨大市场。
研发硬实力,深圳再生筑牢行业竞争壁垒
深圳再生细胞集团能够率先抢占蓝海市场的核心入口,得益于其精心构建的从细胞资源库到临床转化的全产业链生态,和其在洞察市场需求、解决临床难题方面的卓越能力。
在细胞制备这一关键环节,集团凭借前瞻性的战略眼光,在北京、东莞、海南布局了三大GMP标准实验室。针对临床级人脐带间充质干细胞(hUCMSCs)生产的核心痛点,北京再生自主研发的“hUCMSCs主细胞库的制备方法”(专利号:201710374833.8),该技术通过半固体法培养脐带组织块,在显著提高原代培养MSCs得率的同时,有效保留细胞的增殖潜能与分化潜能,更提升了细胞群体均一性。


▲GMP标准实验室
此外,北京再生在临床级hUCMSCs生产全流程中执行严苛质控,生产环境达到B+A级标准,对原辅材料进行严格筛选与管控,建立规范化生产流程与完善的质量管理体系,确保产品可从终端追溯至原始原材料。经专业药理学试验研究与临床前安全性评价验证,该临床级hUCMSCs完全满足治疗糖尿病勃起功能障碍(DIED)的临床质量要求(相关专利:CN202311377729.6),为后续临床转化与广泛应用筑牢技术根基。
此外,在糖尿病健康管理领域的战略布局中,深圳再生集团不仅凭借技术创新构筑核心优势,更依托区域政策红利,在海南博鳌乐城建立海纳(海南)糖尿病医院,为后续技术转化与服务落地搭建起重要载体。同时,围绕新药推进节奏,深圳再生集团正式申请海南博鳌乐城先行区生物医学新技术项目。借助该区域独有的“先行先试”政策优势,包括创新药更早准入、特殊定价机制等,缩短新药商业化周期,推动新药以更快速度进入临床应用场景。


▲海纳(海南)糖尿病医院
全产业布局,助力我国细胞治疗迈向国际前沿
依托“上游细胞药物研发 — 中游生物技术临床转化 — 下游临床应用”的全产业链布局,深圳再生集团正逐步形成“一药领先、多药跟进”的强大管线矩阵,有效带动产业链上下游协同与生态构建,推动产业迈向标准化、规模化发展。
作为国内首款针对“2型糖尿病引起的勃起功能障碍(DIED)”的干细胞1类新药,BJZS001此次获临床试验默示许可,在填补了国内外同适应症干细胞药物的市场空白的同时,也标志着我国在干细胞治疗男科疾病领域实现了里程碑式的突破性进展,为该领域的技术发展划定了新高度。
未来,深圳再生细胞集团将继续加大研发投入,携手投资者、医疗机构等多方合作伙伴探索干细胞在更多慢性病治疗中的应用,为全球生物医疗创新贡献中国力量。
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
-
【关于中秋节的英语手抄报】中秋节是中国传统节日之一,每年农历八月十五庆祝。它不仅是家人团聚的日子,也是...浏览全文>>
-
【关于中秋节的小故事】中秋节是中国传统节日之一,承载着丰富的文化内涵和深厚的情感寄托。自古以来,人们在...浏览全文>>
-
【关于中秋节的文化含义】中秋节,是中国传统节日中最具代表性的节日之一,通常在农历八月十五这一天庆祝。它...浏览全文>>
-
【关于中秋节的手抄报内容】中秋节是中国传统节日之一,象征着团圆与丰收。为了帮助同学们更好地了解中秋节的...浏览全文>>
-
【关于中秋节的诗句古诗】中秋节是中国传统节日之一,自古以来便有赏月、吃月饼、家人团聚的习俗。在众多文人...浏览全文>>
-
【关于中秋节的诗歌】中秋节是中国传统节日之一,自古以来就深受文人墨客的喜爱。许多诗人以中秋为题材,创作...浏览全文>>
-
【关于中秋节的诗词精选】中秋节,是中国传统节日中最具诗意的节日之一。自古以来,文人墨客常以中秋为题,写...浏览全文>>
-
【关于中秋节的来历100字】中秋节,又称月圆节,是中国传统节日之一,时间为农历八月十五。其起源与古代对月亮...浏览全文>>
-
【关于中秋节的句子】中秋节是中国传统节日之一,象征着团圆、思念与丰收。自古以来,文人墨客常用诗句表达对...浏览全文>>
-
【关于张起灵身世年龄介绍】在《盗墓笔记》系列小说中,张起灵是一个神秘而重要的角色,他的身世和年龄一直是...浏览全文>>
