类器官(类似于器官的实验室培养细胞或组织)可作为疾病建模的新工具,但研究人员通常难以复制器官在体内运作的生物物理条件。
来自马萨诸塞州总医院、布莱根妇女医院、Wyss 研究所及其同事的研究小组最近将类器官与器官芯片技术结合起来,复制了常染色体隐性多囊肾病 (APRKD) 的独特疾病过程。
在Science Advances最近的一项研究中,由医学博士 Ken Hiratsuka 和医学博士 Ryuji Morizane 领导的团队报告说,他们使用新的建模系统确定了 APRKD 的两种潜在疗法,目前没有 FDA 批准的治疗方法。
APRKD是一种以肾脏形成囊肿为特征的疾病,囊肿会扩大器官并导致肾功能进行性丧失。据报道,婴儿期死亡率高达30%。对于那些存活下来的患者,41% 的患者需要在 11 岁时进行肾移植。
该疾病的致病基因是 PKHD1,但之前在转基因小鼠模型中对该疾病进行建模的尝试均未成功。研究人员已经能够在实验室中培养突变的 PKHD1 细胞。然而,在静态 3D 类器官中对疾病进行建模是行不通的,因为它是由尿流刺激的细胞表面突变引起的。
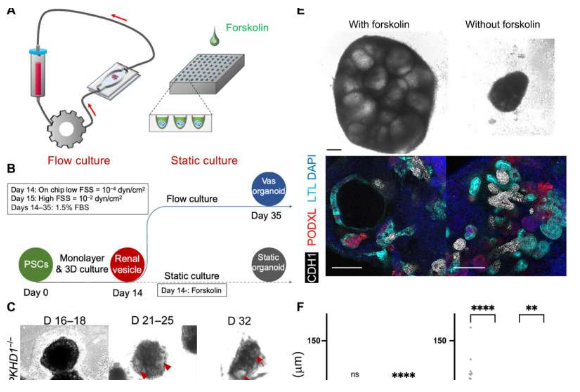
为了克服这一挑战,该团队使用 3D 打印机创建了一个灌注芯片,该芯片模拟了肾脏内细胞的微环境,并允许液体流过类器官。通过这样做,该团队确定了两种机械传感分子(FOS 和 RAC1),它们是该疾病的潜在治疗靶点。
他们还阐明了有关 ARPKD 疾病机制的两个重要问题:
分子 FOS 可能是物种特异性囊肿形成的关键阻止因素,这解释了为什么小鼠模型无法有效复制该疾病
为什么PKHD1基因突变会导致囊肿形成
该团队还测试了两种 FDA 批准的抑制 RAC-1 的药物(R-Naproxen 和 R-Ketorolact)和一种抑制 FOS 的研究性新药(T-5224),这些药物都在这些模型中显示出治疗效果。
标签:
免责声明:本文由用户上传,如有侵权请联系删除!